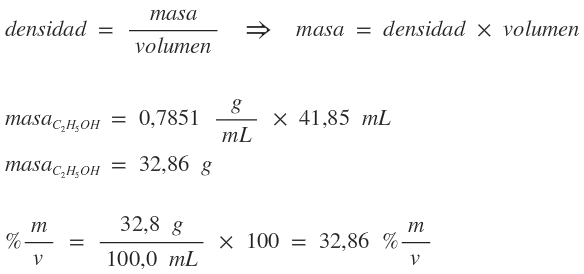26-09-2012, 10:52 PM
Se prepara una solución agregando agua a 41,85 mL de estanol (C2H5OH) hasta un volumen total de 100,0 mL. Si la densidad del etanol puro es 0,7851 g/mL, ¿cuál será la concentración de la solución, expresada en porcentaje de masa en volumen; en gramos por litro y porcentaje en volumen?